A. Un exemple de méthode permettant d'estimer une population
Biodiversité
Elle se décrit à différentes échelles comme celle des
écosystèmes, des espèces ou des individus.On appelle richesse spécifique, le nombre d’espèces présente
dans un milieu. Pour l’estimer, on réalise des échantillonnages :
— piégeage
— observation
— écoute (pour les oiseaux)
— ADN environnemental pour les espèces difficiles à observer.
Biodiversité spécifique chez les coccinelles. Le tableau ci-dessous présente différentes espèces de coccinelles
Variabilité individuelle à l'intérieur d'une espèce de coccinelle, Harmonia axyridis
Taux de variabilité chez les singes anthropoïdes (Homininés et Paninés)
Abondance
L’abondance est une autre composante de la biodiversité.
Elle correspond au nombre d’individus:
— d’une population
— d’une espèce
— d’un taxon (genre, famille, etc…)
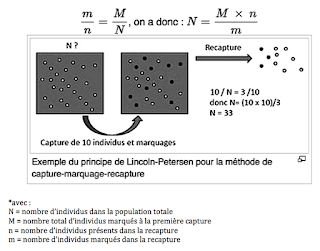
Elle se calcule classiquement par la méthode de « capture-marquage-recapture (CMR) ».
Si on suppose que la proportion d’individus marqués est identique dans l’échantillon
de recapture et dans la population totale, l’effectif de celle-ci s’obtient par
le calcul d’une quatrième proportionnelle (produit en croix).
La méthode de Lincoln -Petersen ou CMR
Intervalle de confiance
À partir d’un seul échantillon, l’effectif d’une population
peut également être estimé à l’aide d’un intervalle de confiance. Une telle
estimation est toujours assortie d’un niveau de confiance strictement inférieur
à 100 % en raison de la fluctuation des échantillons. Pour un niveau de
confiance donné, l’estimation est d’autant plus précise que la taille de l’échantillon
est grande.
Pratiquement, on prendra un intervalle de confiance à 95 %,
— f étant la fréquence du caractère
— n étant l’effectif de l’échantillon :
Application numérique, une histoire de Manchots
On désire évaluer l’abondance d’une population de Manchots
empereurs sur une île au milieu de nulle part. Pour cela, on capture 232 piafs
qui sont marqués puis relâchés. Quelque temps plus tard on recapture 400
bestioles dont 116 sont marquées.
1) Evaluez la population de Manchots empereurs
2) Donnez un intervalle de confiance à 95% de la proportion
d’animaux marqués
3) En déduire un encadrement de l’abondance de Manchots
empereurs dans ce bled paumé.
Correction
1) On applique la formule de Lincoln-Petersen :
N = (M x n)/m
Avec M = 232, n = 400, m = 116
On obtient donc N = 800. La population de l’île est estimée
à 800 Manchots empereurs.
2) L’intervalle de confiance à 95% est donnée par la formule
simplifiée :
I = [f - (1/√N ; f + (1/√N)]
ici N = 800 donc √N = 28,3 et f = 232/800 = 0,29
I = [0,26 ; 0,32]
Cela signifie que le nombre de Manchots marqués dans la
population oscille entre 26% et 32% avec un intervalle de confiance de 95%.
3) On en tire facilement l’encadrement de l’abondance des
oiseaux :
N = M/f – (1/√N) et N = M/f + (1/√N) soit [725 ; 892]
B. L'équilibre de Hardy-Weinberg
Evolution génétique d'une population. L'exemple des loups de Yellowstone
En 1995, le loup, qui avait été éradiqué du Parc de
Yellowstone en 1920, à été réintroduit. Cette réintroduction a permis au
biologiste de suivre l’évolution d’une population à partir du temps 0 et
notamment l’évolution du pool génétique.
Les loups de cette population ont deux couleurs de pelage,
noir ou gris. Ces couleurs sont gouvernées par un gène qui possède deux allèles
qu’on appellera A (noir dominant) et a (gris récessif).
Les loups du parc de Yellowstone
Transmission mendélienne des caractères d'une génération à l'autre
C’est en 1865, que Gregor Mendel a, pour la première fois
mis en évidence le caractère aléatoires de la transmission des caractères d’une
génération à l’autre.
Sachant qu’un individu possède des chromosomes qui vont par
paire, il possède donc une paire d’allèles qui vont déterminer son caractère ou
phénotype. Par exemple, un loup noir sera (A//A ou A//a) puisque A domine sur
a, alors qu’un loup gris sera obligatoirement (a//a). On appelle homozygote un
individu (A//A ou a//a) et hétérozygote un individu (A//a).
Schéma de la transmission aléatoire du caractère "couleur du pelage" chez les loups
Quelques rappels de mathématiques de base pour la génétique des populations
Loi des grands
nombres
Pour un échantillon de taille suffisante, la fréquence
d’apparition d’un caractère f peut être assimilée à sa probabilité d’apparition
p : f = p
Calcul de la
fréquence d’apparition
Un caractère apparaissant n fois dans un échantillon de
taille N possède une fréquence d’apparition de f = n/N
Le modèle de Hardy-Weinberg
C’est en 1908 que Hardy et Weinberg ont, indépendamment,
proposé un modèle d’évolution des fréquences alléliques sur plusieurs
générations pour un gène à deux allèles.
Ce modèle ne peut s’appliquer qu’en tenant compte des
hypothèses suivantes :
— présence d’un grande population
— présence d’une panmixie. Les mâles et le femelle
s’accouplent au hasard. Au début du XXème siècle le comportement animal est très peu connu. C'est à partir des années 1930 que l'éthologie (étude du comportement) va réellement débuter avec Niko Tinbergen, Konrad Lorenz et Karl von Frisch (tous les trois, prix Nobel en 1973). Dans le cas des loups, il n'y a pas de panmixie, puisqu'un couple est formé pour toute la vie.
Donc pas de mâle ou de femelle dominant, pas de super-organisme
(une seule femelle assure la reproduction de toute la colonie comme chez les
abeilles, les termites, les fourmis ou les rats taupes nus dans le cas des
mammifères eusociaux), pas de couple à long terme. Ça restreint déjà
considérablement le champ d’application du modèle !
— absence de migration
— pas de sélection naturelle, alors qu’elle est le moteur de
base de l’évolution
— pas de dérive génétique, ce qui paraît difficile à définir
puisque par définition, c’est un phénomène aléatoire…
Si on appelle p, la fréquence de l'allèle A dans la population et q, la fréquence de l'allèle a, on peut construire le tableau de croisement des individus de la génération 0 et le résultat des génotypes possibles de la génération 1 avec leur fréquence.
Traduit en pourcentage, ça signifie que dans la population
des loups de Yellowstone, il y a :
— 4 % de loups de génotype (A//A)
— 42 % de loups de génotype (A//a)
— 54 % de loups de génotype (a//a)
Nous allons maintenant comparer ces valeurs réelles aux
valeurs théoriques données par l’équilibre de Hardy-Weinberg en n’oubliant
jamais qu’en sciences, le réel a toujours raison sur la théorie.
Calcul de la fréquence des génotypes dans la population de
loups
Si p est la fréquence de l’allèle A dans la population, on
utilise la formule :
p = (nombres (A//A) + ½ (A//a))/ pop. totale
Soit : (31 + 160,5)/765 = 0,25
La fréquence de l’allèle A étant 0,25, la fréquence q de
l’allèle a est obligatoirement
q = 1 - p, soit dans notre cas : 1 – 0,25 = 0,75
Calcul de la fréquence théorique des génotypes en appliquant
l’équilibre de Hardy-Weinberg
Nous savons, d’après l'équilibre de Hardy-Weinberg, que la
fréquence théorique des génotypes est la suivante :
(A//A) = p2 soit dans notre cas,
0,25 x 0,25 = 0,0625
(a//a) = q2 soit dans notre cas,
0,75 x 0,75 = 0,56
(A//a) = 2pq soit dans notre cas,
0,75 x 0,25 x 2 = 0,375
Comparaison entre les résultats pratiques et les résultats
théoriques des fréquences des génotypes
Fréquence des individus (A//A) :
Théorique = 0,065 pratique = 0,04
Fréquence des individus (a//a) :
Théorique = 0,56 pratique = 0,54
Fréquence des individus (A//a) :
Théorique = 0,375 pratique = 0,42
On constate une différence entre les résultats pratiques et
les résultats théoriques. Peut-on tenter d’expliquer ces différences ?
Utilisation de la valeur sélective des génotypes
Cette variable appelée W a été introduite assez récemment en génétique des populations. Elle fait intervenir la capacité de reproduction des animaux (prolificité) et leur espérance de vie. D'autres facteurs de la sélection naturelle interviennent aussi dans le calcul.
On constate que la valeur sélective du génotype A//A est
bien plus faible que celle des autres génotypes.
On observe encore que les loups de génotype a//a sont eux
aussi sous-représentés par rapport à l’équilibre de Hardy-Weinberg.
La faiblesse de la valeur sélective de A//A s’explique par
la faible prolificité de l’animal. On peut supposer que la présence de deux
allèles A est néfaste à l’animal.
La sur-représentation des hétérozygotes s’explique par le
comportement des loups qui s’accouplent préférentiellement entre noirs et gris
Application. Les relations entre drépanocytose et paludisme
Correction
Fréquence p de l’allèle A dans la population de la ville
test :
3182 + 419/4116 = 0,875
D’où fréquence q de l’allèle S :
1-0,875 = 0,125
Fréquence du génotype A//A selon l’équilibre de H-W :
f = p2 = 0,765
Fréquence du génotype S//S
f = q2 = 0,0156
Fréquence du génotype A//S
f = 2pq = 0,218
Nombre théorique d’enfants A//A
350 000 x 0,765 = 267 969
Nombre théorique d’enfants A//S
350 000 x 0,218 = 76300
Nombre théorique d’enfants S//S
350 000 x 0,0156 = 5460
Comparaison des résultats réels et théoriques :
A//A 270
550 contre 267 969, soit une différence de 1% environ, qui est négligeable
A//S
71400 contre 76563, soit une différence de 7% tout à fait acceptable
dans ce type de calcul
S//S
8050 contre 5468, soit une différence de 33%.
Il y a donc 33% de naissances en plus d’individus S//S que prévues par la théorie.
Cette différence provient du fait que les individus S//S
sont protégés contre la paludisme par la drépanocytose. Le nombre de décès est
donc largement inférieur à ce que prévoit la théorie. En outre, la protection
des individus A//S contre le paludisme et l’absence de symptôme drépanocytaire
permet le maintien de l’allèle S, allèle morbide, dans la population.
Si on étudie le génotype des afro-américains, on constate la
quasi absence de l’allèle S, alors qu’ils sont les descendants d’esclaves
africains arrivés en Amérique au cours du XVIIIème et du XIXème siècle. Cette
disparition s’explique par la faible présence du paludisme an Amérique du Nord.
L'impact des activités humaines sur la biodiversité
Nous savons que l’activité humaine perturbe l’activité des
écosystèmes par les différentes pollutions, par l’extension des aires urbaines
et par l’implantation de constructions dans des zones à biodiversité importante.
Nous allons nous intéresser plus précisément à l’implantation
de routes et d’obstacles dans une zone déterminée, entrainant sa fragmentation.
Dérive génétique
La dérive
génétique est l'évolution d'une population ou d'une espèce
causée par des événements aléatoires,
impossible à prévoir. Du point de vue génétique,
c'est la modification de la fréquence d'un allèle,
ou d'un génotype, au sein d'une population,
indépendamment des mutations, de la sélection naturelle et des migrations.
La dérive génétique est causée par
des événements aléatoires et imprévisibles, comme le hasard des
rencontres des spermatozoïdes et des ovules,
dans le cas d'une reproduction sexuée. La théorie de la dérive
génétique a été établie par Motoo
Kimura en 1968.
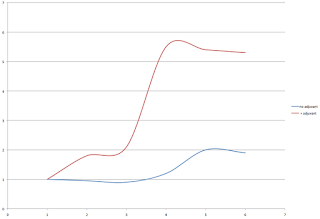
On peut constater plusieurs choses :
— plus la population est petite plus la dérive génétique est
importante.
— dans certains cas, la limitation de la population est
telle que des allèles peuvent disparaître et abaisser la variabilité génétique
de l’espèce considérée
— l’abaissement de la variabilité génétique et l’endogamie
entrainent des phénomènes de consanguinité. La baisse du taux de fécondité peut
entrainer la disparition de la population.